LILLY
盐酸度洛西汀肠溶胶囊
用于治疗抑郁症。用于治疗广泛性焦虑障碍。
盐酸度洛西汀肠溶胶囊-说明书
介绍
主要成份:主要组成成分盐酸度洛西汀。 化学名称:(+)-(S)-N-甲基-γ-(1-萘基氧)-2-噻吩丙醇胺盐酸盐 化学结构式: 分子式:C18H19NOS·HCl 分子量:333.88
用法用量:和
性状:本品内容物为白色或类白色球状肠溶颗粒。 60mg*胶囊:不透明绿色囊体和蓝色囊帽,囊体壳上印“60mg”。
详细说明书
温馨提示:部分商品说明书更换频繁,请以商品实物为准
请仔细阅读以盐酸度洛西汀肠溶胶囊说明书并按照说明使用或在医生与药师指导下购买和使用。
| 【通用名称】 | 盐酸度洛西汀肠溶胶囊 |
| 【药品名称】 | 盐酸度洛西汀肠溶胶囊 |
| 【主要成份】 | 主要组成成分盐酸度洛西汀。 化学名称:(+)-(S)-N-甲基-γ-(1-萘基氧)-2-噻吩丙醇胺盐酸盐 化学结构式: 分子式:C18H19NOS·HCl 分子量:333.88 |
| 【功能主治】 | 用于治疗抑郁症。用于治疗广泛性焦虑障碍。 |
| 【用法用量】 | 和 |
| 【性状】 | 本品内容物为白色或类白色球状肠溶颗粒。 60mg*胶囊:不透明绿色囊体和蓝色囊帽,囊体壳上印“60mg”。 |
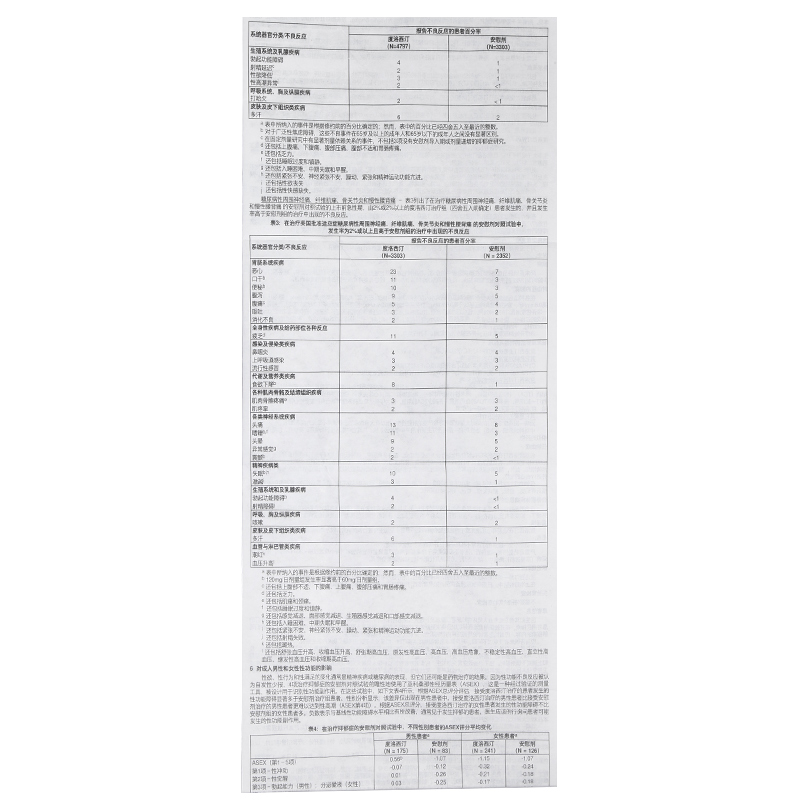
| 【不良反应】 | 表见说明书 注解: 此数据来源于2011年10月19日前安慰剂对照的数据库,包括已批准的适应症及其它条件下已完成的临床研究。 包括应激性、急迫性和混合性尿失禁。 包括慢性背痛和骨关节炎。 上腹部疼痛、下腹部疼痛、腹部压痛、腹部不适、胃肠道疼痛。 包括腹泻出血、下胃肠道出血、呕血、便血、肛门出血、黑粪症、直肠出血、溃疡出血。 包括无力。 在年长患者中跌倒更加普遍(≥65岁) 包括收缩压升高、舒张压升高、收缩期高血压、舒张期高血压、高血压危象、原发性高血压和高血压。 丙氨酸氨基转移酶(ALT)升高、肝酶升高、天门冬氨酸氨基转移酶(AST)升高、肝功能测试异常、γ-氨基丁酸氨基转移酶升高、血碱性磷酸酶升高、血胆红素升高、肝酶异常。 包括厌食症。 肌肉骨骼僵硬。 肌痛、颈痛。 睡眠过度、镇静。 包含感觉减退,面部感觉减退,生殖器感觉迟钝和口腔感觉异常。 中段失眠、终期失眠症和初段失眠。 包含快感缺失。 性欲缺乏。 紧张不安感、坐立不安、紧张、精神运动过度。 意识模糊状态。 梦魇。 射精失败。 包括热潮红。 一般不良反应头晕、恶心、头疼,也见于度洛西汀停药后,发生率≥5%。在安慰剂对照的临床试验中,度洛西汀治疗伴随小的ALT、AST、肌酸磷酸激酶(CPK)和钾离子从基线至终点平均值升高;与对照组相比,度洛西汀治疗的患者可有罕见的、暂时的异常值。 血糖调整―在3项治疗糖尿病周围神经痛的临床试验中,平均糖尿病持续时间为12年,平均空腹血糖基线值为176mg/dL,平均糖化血红蛋白(HbA1c)基线值为7.81%。在这3项试验的最初12周急性治疗期,度洛西汀治疗组患者的空腹血糖可见小幅升高。HbA1c在度洛西汀治疗组和安慰剂对照组均稳定。在治疗持续到52周时,度洛西汀治疗组和安慰剂组均出现HbA1c升高,度洛西汀治疗组平均增高值比安慰剂组高0.3%。尽管常规治疗组患者显示轻度降低,但空腹血糖和总胆固醇显示小幅增高。 停药后,有报告停药后症状,最常见报告的症状包括下列临床试验中突然停服或逐渐停服度洛西汀,有头晕、恶心、头疼、感觉异常、疲劳、呕吐、兴奋、梦魇、失眠、腹泻、焦虑、多汗、眩晕、嗜睡和肌痛。 上市后使用度洛西汀治疗出现的自发不良反应报告 下列不良反应发生率(<0.01%): 心脏疾患:室上性心律失常。 耳及迷路障碍:治疗终止后耳鸣 内分泌失调:不良反应包括抗利尿激素分泌过多综合症。 眼疾:青光眼。 胃肠疾病:显微镜下结肠炎。 肝胆管疾患:肝炎、黄胆。 免疫系统紊乱:过敏反应、超敏反应。 实验室检查:ALT升高、碱性磷酸酶升高、AST升高、胆红素升高。 代谢、营养障碍:低钠血症、高血糖(尤其是糖尿病患者)。 骨骼、结缔组织疾病:牙关紧闭症。 神经系统障碍:锥体外系综合症、停药时感觉异常(包括类似电击样感觉)不宁腿综合征、5-羟色胺综合症、癫痫发作、停药后癫痫发作。 精神病性障碍:躁狂症、攻击和发怒(尤其在治疗早期或治疗停止后)。 皮肤及皮下组织症状:血管神经性水肿、暗伤、皮肤脉管炎(有时伴有系统受累)、瘀斑、Stevens-Johnson综合症、荨麻疹。 血管病症:直立性低血压(尤其在开始治疗时)、晕厥(尤其在开始治疗时)、高血压危象。 生殖系统和乳腺障碍:妇产科出血、溢乳、高催乳素血症。 下列不良反应发生率(≥0.01%-<0.1%): 精神病性障碍:幻觉。 肾、泌尿系统紊乱:尿潴留。 皮肤及皮下组织症状:皮疹。 |
| 【用药禁忌】 | 过敏 度洛西汀肠溶胶囊禁用于已知对度洛西汀或产品中任何非活性成分过敏的患者。 单胺氧化酶抑制剂 由于增加发生五羟色胺综合征的危险,所以将要服用本品治疗精神疾病或停用本品5天内,禁用MAOI。MAOI停药14天内也应禁用本品。 由于增加发生五羟色胺综合征的危险,所以正在使用MAOI(如利奈唑胺或静脉注射亚甲基蓝)的患者也应禁用本品。 未经治疗的窄角型青光眼 临床试验显示,度洛西汀有增加瞳孔散大的风险,因此,未经治疗的窄角型青光眼患者应避免使用度洛西汀。 |
| 【注意事项】 | ,终止度洛西汀治疗风险的描述)。 使用抗抑郁药物治疗的抑郁症和其它适应症的患者,包括精神病性和非精神病性障碍,患者的家人和照料者应该警惕,需要对患者出现的激越、易怒、行为异常改变、出现自杀行为以及上面提及的其他症状进行监测,一旦出现这些症状立即向卫生保健机构提供信息,这些监测也应包括家人或照料者的每日观察。度洛西汀肠溶胶囊开处方时应予以治疗剂量的最小量,以减少过量的风险。 筛查双相障碍患者:抑郁发作可能是双相障碍的早期表现。通常认为(虽然未经对照研究证实),单用抗抑郁药物治疗抑郁发作可能会增加双相障碍患者的混合/躁狂发作。虽然无法预测会出现以上提及的哪一项症状,但是,在抗抑郁药物治疗前,应对抑郁患者进行适当地筛查,确定是否患有双相障碍的风险。筛查方法包括详细地询问精神病病史,有无自杀行为、双相障碍和抑郁的家族史。应注意度洛西汀尚未批准用于治疗双相抑郁。 肝脏毒性 有报道度洛西汀治疗患者中出现肝功能衰竭,有时是致命性的。这些病例表现为伴有腹痛、肝肿大、伴有或无黄疸的氨基转移酶升高超过正常值上限20倍的肝炎。服用度洛西汀的患者如果出现黄疸或其它有临床显著意义的肝功能障碍时,应停用度洛西汀,而且不应该继续治疗,除非有其它的原因。 也有出现氨基转移酶无明显升高的胆汁郁积型黄疸病例的报道。上市后报告显示氨基转移酶、胆红素和碱性磷酸酶升高也发生在患有慢性肝病或肝硬化患者中。 在研发研究中,度洛西汀有增加血清氨基转移酶水平的风险。该酶升高导0.3%(92/34756)度洛西汀治疗的患者中断治疗。这些患者出现氨基转移酶升高的时间中位数为2个月。所有适应症的安慰剂对照研究中,度洛西汀组中有1.25%(144/11496)的患者ALT升高超过正常上限3倍以上,而安慰剂组中为0.45%(39/8716)。固定剂量的安慰剂对照研究中,有证据显示ALT升高超过正常上限3倍和AST升高超过正常上限5倍,与药物剂量有量效关系。 因为度洛西汀和酒精的相互作用可能引起肝损害或者加剧已有的肝病恶化,所以度洛西汀通常不用于有大量饮酒和慢性肝病患者的治疗。 直立性低血压、跌倒和晕厥 使用治疗剂量度洛西汀治疗时有直立性低血压、跌倒和晕厥的报道。通常发生在治疗的第一周内,也可以发生治疗的任何时期,特别是增加剂量以后。跌倒的发生与直立性血压降低的程度有关,同时还与其他可能增加潜在跌倒风险的因素有关。 对所有参加安慰剂对照研究的患者进行分析,度洛西汀组患者的跌倒率高于安慰剂组。跌倒风险与直立性血压降低的发生有关。患者同时服用其它引起直立性低血压药物(如降血压药)或强CYP1A2酶抑制剂,以及服用度洛西汀剂量超过60mg/日时,发生血压下降的危险增加。患者接受度洛西汀治疗时如果发生直立性低血压、跌倒和晕厥,应考虑降低剂量或者停药。 跌倒风险与患者具有的跌倒相关的潜在风险成正比,且随着年龄的增长而增加。因为合并用药、共存疾病和步态紊乱等风险因素在老年人中更普遍的存在,导致老年人具有更高的潜在跌倒风险,所以年龄增长本身对跌倒的影响尚不清楚。已报道的跌倒的严重后果包括骨折和住院治疗。 五羟色胺综合征 SNRI和SSRI单药治疗时,曾有发展成五羟色胺综合征的报道,这两种情况会威胁生命。使用度洛西汀时也会出现上述两种情况,特别是在合并使用其他五羟色胺药(包括曲坦类、三环类抗抑郁药、芬太 尼、锂盐、曲马多、色氨酸、丁螺环酮和圣约翰草)和损害五羟色胺代谢药(特别是MAOI,拟定用于治疗精神疾病和其他情况,如利奈唑胺或静脉注射亚甲基蓝)。 五羟色胺综合征包括精神状态改变(如激越、幻觉、精神错乱和昏迷)、自主神经功能不稳定(如心动过速、血压不稳、头晕、发汗、脸红和高热)、神经肌肉症状(如震颤、强直、肌痉挛、腱反射亢进、共济失调)、癫痫发作和/或胃肠道症状(如恶心、呕吐、腹泻)。需要监测患者五羟色胺综合征。 禁止度洛西汀与MAOI合并使用治疗精神疾病。正在使用MAOI(如利奈唑胺或静脉注射亚甲基蓝)的患者不应该开始服用本品。所有关于亚甲基蓝给药途径的报告均为静脉给药,剂量范围为1mg/kg-8mg/kg。没有报告亚甲基蓝的其他给药途径(如口服片剂或局部组织注射)或更低剂量。必要时,正在服用本品的患者可能需要MAOI治疗(如利奈唑胺或静脉注射亚甲基蓝)。开始使用MAOI治疗前应该停用本品。 如果临床上需要合并使用度洛西汀和其他五羟色胺药(包括曲坦类、三环类抗抑郁药、芬太 尼、锂盐、曲马多、色氨酸、丁螺环酮和圣约翰草),应该让患者意识到潜在的增加发生五羟色胺综合征的危险,特别是开始治疗和增加剂量时。 如果上述事件发生,需要立即停用度洛西汀和任何合并使用的五羟色胺药物,并开始支持性的对症治疗。 异常出血 包括度洛西汀在内的SSRI和SNRI会增加出血事件的风险。合并使用阿斯匹林、非甾体抗炎药(NSAID)、华法林和其它抗凝剂会增加这种风险。病例报道和流行病学研究(病例对照和队列研究)证明使用干扰5-羟色胺再摄取的药物和胃肠道出血之间有联系。出血事件从斑状出血、血肿、鼻衄、瘀点到威胁生命的出血。 患者合并使用度洛西汀和NSAID、阿斯匹林或其它影响凝血功能药物时,需要关注出血的危险。 严重的皮肤反应 使用度洛西汀时可能出现严重的皮肤反应包括多形性红斑和Stevens-Johnson综合症(SJS)。度洛西汀相关的SJS报告率超过出现严重皮肤反应的总人口背景发生率(每一百万人中出现1~2例)。由于少报,普遍认为该报告率被低估了。 出现水泡、脱皮性皮疹、粘膜溃疡或没有其他病因确定的过敏症状时,应停止服用度洛西汀。 度洛西汀停药 已对度洛西汀的停药症状做过系统研究。在安慰剂对照试验中,骤停药物或缓慢停药时,观察到度洛西汀治疗的患者发生率大于或等于1%,且度洛西汀治疗的患者发生率明显高于停用安慰剂患者的症状包括:头晕、头痛、恶心、腹泻、感觉异常、易激惹、呕吐,失眠、焦虑、多汗和疲劳。 其他SSRI和SNRI上市以来,有自发性报告因为停用上述药物而引起的药物不良反应,尤其是骤停药物后出现的,包括:恶劣心境、易激惹、激越、头晕、感觉紊乱(感觉异常和电击感)、焦虑、意识模糊、头痛、情感脆弱、乏力、失眠、轻躁狂、耳鸣、癫痫等。虽然上述不良反应具有自限性,但有些很严重。 停用度洛西汀后应注意观察患者有无上述症状的出现。建议尽可能的逐渐减药,而不是骤停药物。由于减少药物剂量或停药而引起了无法耐受的症状时,可以考虑应用以往的处方剂量。然后,临床医生再以一个更慢的速度减药。 促发躁狂/轻躁狂 在治疗抑郁症的安慰剂对照试验中,度洛西汀组中有0.1%(4/3779)的患者转为躁狂/轻躁狂,安慰剂组为0.04%(1/2536)。在治疗广泛性焦虑障碍的安慰剂对照实验中,没有报告出现躁狂/轻躁狂行为。据报道,用其他已上市的抗抑郁药物治疗的一小部分患者转为躁狂/轻躁狂。与其他抗抑郁药一样,既往有躁狂史的患者慎用度洛西汀。 癫痫 尚未系统评价度洛西汀在癫痫患者中的疗效,临床试验中排除这些患者。在安慰剂对照临床试验中,度洛西汀组中有0.02%(3/12722)的患者出现癫痫发作,而安慰剂组为0.01%(1/9513)。既往有癫痫发作史的患者慎用度洛西汀。 对血压的影响 在各种适应症的安慰剂对照临床研究中,度洛西汀治疗引起血压升高,收缩压平均升高0.5mmHg,舒张压平均升高0.8mmHg,安慰剂组收缩压平均升高0.6mmHg,舒张压平均升高0.3mmHg。持续升高的频率(连续3次随访)无显著差别。一项评估度洛西汀的多种效果,包括超过治疗剂量(加速剂量滴定)对血压影响的临床药理研究显示,在剂量增加到200mg每日两次的过程中,卧位血压增高。在最高剂量(200mg每日两次)到服药12小时,平均脉搏增加5.0到6.8次,平均收缩压升高4.7到6.8mmHg,平均舒张压升高4.5到7.0mmHg。 治疗开始前应测量血压,治疗后也应定期测量血压。 临床重要的药物相互作用 度洛西汀主要通过CYP1A2和CYP2D6代谢。 其它药物对度洛西汀的潜在影响: CYP1A2抑制剂-应避免度洛西汀合并使用强CYP1A2抑制剂。 CYP2D6抑制剂-度洛西汀合并使用强CYP2D6抑制剂时会出现血药浓度增加(平均60%)。 度洛西汀对其它药物的潜在影响: CYP2D6代谢的药物-度洛西汀与主要由CYP2D6代谢并且治疗指数窄的药物合并使用时要慎重,这些药物包括三环类抗抑郁药(TCA)(包括去甲替林、阿米替林和丙咪嗪),吩噻嗪和1C类抗心律失常药(如普罗帕酮、氟卡胺)。如果TCA和度洛西汀一起使用,需要监测TCA的血药浓度,并减少TCA的用量。因为甲硫达嗪血药浓度增高会有严重室性心律不齐和猝死的风险,度洛西汀不能和甲硫达嗪一起使用。 其它重要的药物相互作用: 酒精-大量饮酒同时服用度洛西汀与严重肝脏损害相关,所以有大量使用酒精的患者通常不能处方度洛西汀。 中枢神经系统(CNS)活性药物-度洛西汀主要作用于中枢神经系统,与其它中枢活性药物使用时要慎重,包括作用机制相似的药物。 低钠血症 包括度洛西汀在内的SSRI和SNRI治疗会发生低钠血症。在许多病例中,这种低钠血症似乎是不适当抗利尿激素分泌综合征(SIADH)的结果。有血钠浓度低于110mmol/L的病例报告,停用度洛西汀后可逆转。老年患者服用SSRI和SNRI时出现低钠血症的危险很高。患者出现低钠血症时需要考虑停药,并进行合适的治疗。 低钠血症的症状包括头痛、集中注意力困难、记忆损害、意识模糊、衰弱及摇摆,这会导致摔跤。更严重和/或紧急的情况有幻觉、昏厥、癫痫发作、昏迷、呼吸停止和死亡。 合并躯体疾病患者的用药 在合并系统性疾病患者中使用度洛西汀的经验有限。尚无胃动力改变对度洛西汀肠溶包衣稳定性影响的资料。在极端的胃酸环境下,如果没有肠溶包衣保护,可能会水解形成萘酚。在胃排空减慢的患者(如某些糖尿病患者)中使用度洛西汀时需要小心。 度洛西汀在近期有心肌梗死病史或不稳定冠状动脉疾病中使用没有得到系统研究,因为上市前的研究中一般会排除此类患者。 肝功能不全-度洛西汀通常不应该用于此类患者。 严重肾功能损害-度洛西汀通常不应该使用于终末期肾病或严重肾脏损害的患者(肌酐清除率<30mL/分)。在终末期肾病(需要透析)患者中,血浆度洛西汀,尤其是它的代谢产物浓度增高。 已得到控制的窄角性青光眼-临床试验显示,度洛西汀有增加瞳孔散大的风险,因此,度洛西汀慎用于已控制的窄角性青光眼患者。 尿迟疑和尿潴留 度洛西汀是一类可影响尿道阻力的药物。如果度洛西汀治疗过程中出现尿迟疑,需要考虑可能与药物有关。 上市后经验表明,有尿潴留病例。如果度洛西汀治疗过程中出现尿潴留,某些情况下需要住院和/或导尿。 实验室检查 不需要特别的实验室检查。 患者信息 医生和其他卫生专业人员应告知患者、家属及照料者度洛西汀治疗的获益和风险,建议他们合理用药。有给患者提供的“在儿童青少年中使用抗抑郁药的用药指南”,医生和卫生专业人员应向患者、家属或照料者介绍阅读用药指南,协助他们了解其中的内容。应当给患者讨论用药指南的机会,并能就患者提出的问题给出回答。 应当告诫患者注意以下问题,并且要求患者服用度洛西汀时,如果发生了这些问题,及时向医生报告。 自杀想法和自杀行为-患者、家属及其照料者应当对下列问题提高警惕:焦虑、激越、惊恐发作、失眠、易怒、敌视、攻击、冲动、静坐不能(精神运动性不安)、轻躁狂、躁狂、行为异常改变、抑郁加重、轻生想法,尤其是在抗抑郁药治疗早期和上调或下调剂量时。由于这些改变常突然发生,应告诫患者家属和照料者每天观察这些症状。应当向患者的医生或卫生专业人员报告这些症状,尤其是当这些症状极其严重、突然发生或不是患者平时的症状表现时。可能导致自杀想法和行为风险升高的这些症状需要密切监测,甚至可能改变治疗。 度洛西汀肠溶胶囊应整体吞服,既不能嚼碎或压碎,也不能洒在食物上或混在饮料中,因为这样有可能影响肠溶包衣。 继续治疗处方-患者可能会注意到度洛西汀治疗1到4周症状改善,但他们需要继续治疗。 肝脏毒性-应告知患者度洛西汀治疗的患者中曾报告严重肝脏问题,有时是致命问题。如果患者服用本品期间出现可能为肝脏问题的征兆:发痒、右上腹痛、尿色加深或皮肤/眼睛发黄,这些现象,应告知其保健医师。服用本品期间大量饮酒可能引起严重肝脏损伤。 异常出血-度洛西汀合并使用阿斯匹林、NSAID、华法林和其它抗凝剂会增加出血的风险。 严重的皮肤反应-患者需要注意度洛西汀可能引起严重的皮肤反应。严重的皮肤反应可能需要入院治疗,也许会危及生命。如果患者出现皮肤水泡、脱皮性皮疹、口疮、荨麻疹或其它过敏反应,应该立即联系他们的医生或获得急诊帮助。 合并用药-由于药物之间的相互作用,患者需要被告知如果正在或计划服用其他处方或非处方药物时,要通知其医生。 五羟色胺综合征-合并使用度洛西汀和其他五羟色胺药(包括曲坦类、三环类抗抑郁药、芬太 尼、锂盐、曲马多、丁螺环酮、色氨酸和圣约翰草)时需要注意发生五羟色胺综合征的危险。 应该告知患者五羟色胺综合征的相关征兆和症状,包括精神状态改变(如激越、幻觉、精神错乱和昏迷)、自主神经功能不稳定(如心动过速、血压不稳、头晕、发汗、脸红和高热)、神经肌肉症状(如震颤、强直、肌痉挛、腱反射亢进、共济失调)、癫痫发作和/或胃肠道症状(如恶心、呕吐、腹泻)。如果患者出现这些症状,应立即采取药物治疗。 停药-患者停药可能出现头晕、头疼、恶心、腹泻、感觉异常、易怒、呕吐、失眠、焦虑、多汗和疲劳症状,应该建议患者不要改变剂量方案或未咨询医生自行停药。 躁狂或轻躁狂行为-对于具有抑郁症状的患者,在开始本品治疗前应该充分筛查其双向障碍(如自杀家族史、双向障碍和抑郁)的风险。建议患者报告任何躁狂反应的征兆或症状,如精力极其旺盛、严重的睡眠问题、思维奔逸、不计后果的行为、言语增加或语速加快、异乎寻常的想法以及过度高兴或兴奋。 癫痫-如果患者具有癫痫病史,应建议告知医生。 对血压的影响-警告患者本品可能引起血压升高。 低钠血症-告知患者曾报告SNRI和SSRI治疗(包括度洛西汀)引起的低钠血症。告知患者钠血症的征兆和症状。 合并躯体疾病-患者应该告知医生其所有的疾病情况。 尿迟疑和尿潴留-本品可能影响排尿。如果患者出现尿流速问题,应咨询医生。 怀孕和哺乳-出现以下情况时,患者需要咨询医生: · 治疗过程中怀孕 · 治疗过程中计划怀孕 · 哺乳 酒精-虽然度洛西汀不会加重酒精所造成的精神或运动技巧损害,但大量饮酒同时服用度洛西汀与严重肝脏损害相关。所以大量饮酒的患者通常不能服用度洛西汀。 直立性低血压、跌倒和晕厥-患者需要被告知出现直立性低血压、跌倒和晕厥的风险,特别是开始治疗和剂量增加时,还有同时服用其它会促进直立性低血压的药物。 精神活动表现的干扰-任何影响精神的药物都会损害判断力、思维或运动能力。尽管在对照研究中并未发现度洛西汀会损害精神行为、认知功能或记忆力,但由于度洛西汀的可能引起镇静作用和头晕,在操作危险机械包括机动车时应加以注意。除非患者能确定度洛西汀对其该方面的能力没有影响。 |
| 【相互作用】 | 可能影响度洛西汀的其他药物 度洛西汀的代谢与CYP1A2和CYP2D6有关 CYP1A2抑制剂-度洛西汀与氟伏沙明(强CYP1A2抑制剂)联合应用于男性受试者(n=14)时,度洛西汀 AUC增加超过5倍,Cmax增加约2.5倍,T1/2增加约3倍。其他对CYP1A2代谢有抑制作用的药物包括:西米替丁,喹诺酮类抗生素例如环丙沙星, 依诺沙星。 CYP2D6抑制剂-由于CYP2D6参与度洛西汀的代谢,所以合并使用度洛西汀和强CYP2D6抑制剂时,盐酸度洛西汀的药物浓度将会增加,(见[注意事项]项下药物相互作用)。 度洛西汀可能影响的其他药物 通过CYP1A2代谢的药物-体外药物相互作用研究显示:度洛西汀对CYP1A2活性无诱导作用。因此,虽然未进行有关酶诱导作用的临床研究,预计不会因为酶诱导作用而使CYP1A2底物(例如茶碱、咖啡 因)的代谢增加。虽然体外研究显示度洛西汀是CYP1A2抑制剂,但是度洛西汀(60 mg 每日两次给药)与作为CYP1A2底物的茶碱联合使用时,茶碱的药代动力学没有明显变化。因此,度洛西汀对CYP1A2底物的代谢不可能产生具有临床意义的明显影响 |
| 【贮藏条件】 | 15~30℃室温保存 |
| 【批准文号】 | 注册证号H20150287 |
| 【生产企业】 |
盐酸度洛西汀肠溶胶囊-相关科普
更多相似功效药品推荐
更多热门药品
知名品牌
搜索热点